Boc-His(Trt)-Aib-Gln(Trt)-Gly-OH
Boc-His(Trt)-Aib-Gln(Trt)-Gly-OH
Fuerschungsapplikatioun:
Dëst geschützt Tetrapeptid gëtt an der Peptidsynthese a Konformatiounsstudien agesat. D'Integratioun vun Aib (α-Aminoisobuttersäure) erlaabt et de Fuerscher, helix Strukturen a Faltverhalen a kuerze Peptiden z'ënnersichen. Déi geschützt funktionell Gruppen (Boc, Trt) garantéieren Stabilitéit a Selektivitéit während der Festphas-Peptidsynthese, wat et zu engem wäertvolle Modell fir d'Studium vun der Peptid-Réckgratdynamik an den Interaktioune tëscht Säiteketten mécht.
Funktioun:
Boc-His(Trt)-Aib-Gln(Trt)-Gly-OH déngt als Modellverbindung fir d'Peptidstabilitéit a strukturell Motiver z'ënnersichen. Aib dréit zur helixer Stabiliséierung bäi, während Histidin- a Glutaminreschter potenziell Interaktiounsplaze bidden, déi nëtzlech sinn beim Design vu bioaktive Peptiden oder beim Imitéiere vu Proteinfragmenter. Et kann och e Virleefer fir funktionell Peptiden an der Medikamentenentwécklung oder biochemeschen Tester sinn.





![Fmoc-L-Lys[Ste(OtBu)-γ-Glu-(OtBu)-AEEA-AEEA]-OH](https://cdn.globalso.com/gentolexgroup/Glepaglutide9-300x300.png)
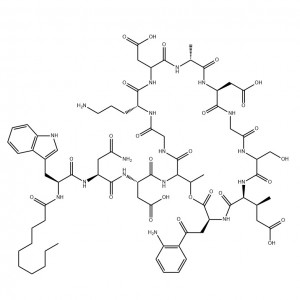
![Fmoc-L-Lys[Eic(OtBu)-γ-Glu(OtBu)-AEEA]-OH](https://cdn.globalso.com/gentolexgroup/Glepaglutide10-300x300.png)

